今日分享 | 药物临床试验期间方案变更技术指导原则

药物临床试验期间方案变更是指药物临床试验期间,因各种原因,需要对药品审评机构已批准或经沟通交流认可的临床试验方案内容进行修改或完善。申办者承担临床试验方案变更的主体责任,全面、深入评估临床试验期间方案变更的必要性和科学合理性,评估方案变更对受试者安全的影响。为指导申办者更好地开展临床试验期间方案变更的安全性评估及相关工作,控制临床试验风险,保护受试者安全,国家药品监督管理局药品审评中心(CDE)制定本指导原则。
02
方案变更的常见情形
与评估要点
1. 临床试验期间,发现药物新的安全性问题或潜在安全风险,如临床或非临床研究中新的安全性数据与信息等,需要及时对临床试验安全性研究相关内容进行修改或完善;
2. 临床试验期间,需要对临床试验有效性研究相关内容 进行修改或完善;
3. 临床试验期间,为了提高临床试验实施效率,需要修改试验方案中相关内容;
4. 其他,如变更联系人、联系方式等,一般不涉及试验方案设计的变化。
1. 临床试验受试者的安全风险(包括风险-获益权衡);
03
变更分类
分为实质性变更和非实质性变更。
对临床试验受试者的安全性、试验的科学性、试验数据的可靠性可能产生显著性影响的变更。
(2)变更主要终点或对试验安全性、科学性有重要影响的次要终点;
(3)变更主要终点、重要次要终点的测定方法或评价标准;
(4)变更可能对试验科学性、安全性有显著性影响的入选标准或排除标准,如明显改变受试人群特征或范围等;
(6)变更给药方法,如给药时间、给药间隔时间、给药周期等;
(7)变更、增加或删除对照组/对照药物(包括安慰剂);
(8)变更可能对试验安全性、科学性有重要影响的诊断、医疗监测方法或程序;
(9)变更可能对试验安全性、科学性有重要影响的基础治疗;
(11)变更试验结束的定义、暂停试验标准、终止试验 标准(包括受试者个体试验终止和整个临床试验终止);
(12)变更偏倚控制方法,如随机化方法、盲法设置等;
(13)变更主要终点或重要次要终点的统计分析方法、分析计划;
(14)撤销数据安全监查委员会/数据监查委员会/独立数据监查委员会;
2. 文字表述的微小调整,以澄清方案中表述不明确的内容;
3. 记录试验数据的文件格式或内容(非实质性内容)的适当调整;
5. 基于预防目的而不是紧急风险控制情况下增加安全性指标或访视次数(侵入性检查除外);
7. 其他。
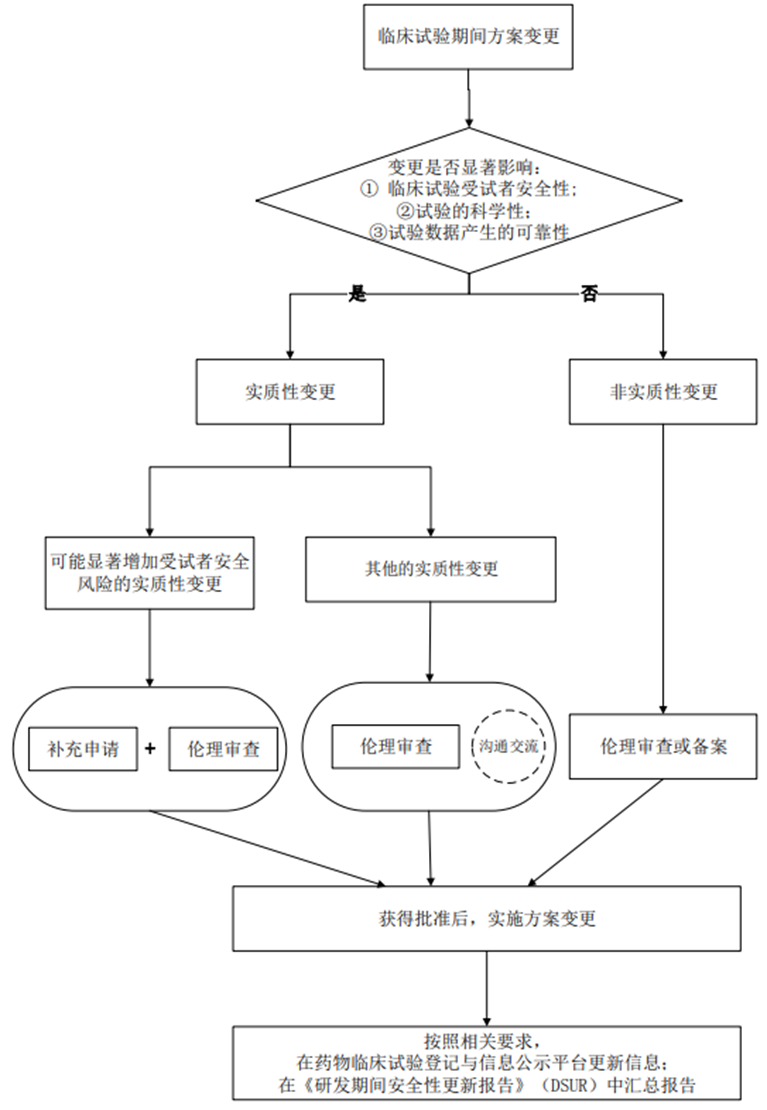
04
变更流程